一、概览:ISO 13485:2016是 2016年发布的医疗器械行业专用质量管理体系,适用于医疗器械全生命周期(设计开发、生产、存储分销、安装服务等)相关组织,核心是通过风险管理贯穿全程,建立覆盖质量管理体系、管理责任、资源管理、产品实现、测量分析与改进五大核心模块的管控要求,明确文件控制、记录保存(至少产品寿命期或放行后2 年)、设计开发验证确认、供应商管理、不合格品控制等关键环节的刚性要求,确保医疗器械安全有效并符合全球法规合规要求。二、思维导图:
三、详细总结
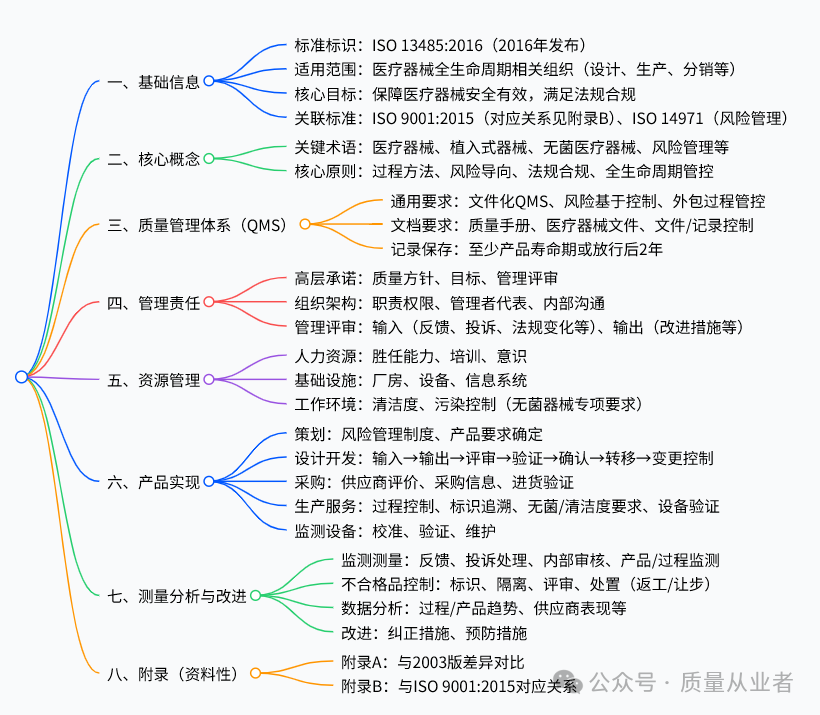
1、基础信息与适用范围
标准定位
标准名称:ISO 13485:2016《Medicaldevices - management systems - Re for regulatorypurposes》发布时间:2016 年 3 月 1 日,替代 ISO13485:2003 及 ISO/TR 14969:2004核心定位:医疗器械行业专用质量管理体系标准,侧重法规合规性,适用于全球医疗器械相关组织的注册、认证及体系核查。适用范围
适用对象:涉及医疗器械全生命周期(设计开发、生产、存储分销、安装、服务、报废处置)的组织,包括制造商、供应商、进口商、分销商等。产品覆盖:所有类型医疗器械(含植入式、无菌、体外诊断器械等),无论组织规模大小。特殊说明:可排除不适用的条款(如设计开发控制),但需提供正当理由并记录。2、核心概念与原则
关键术语定义
| 术语 |核心定义 ||| 医疗器械 |用于人体诊断、治疗、监测等目的的仪器、设备、软件、材料等,非通过药理 / 免疫 /代谢方式发挥主要作用 || 植入式医疗器械 | 需通过医疗 /手术干预才能取出,植入人体后停留≥30 天 || 无菌医疗器械 |预期满足无菌要求的医疗器械 || 风险管理 |系统应用政策、程序,对风险进行分析、评估、控制和监测的过程 || 投诉 |针对医疗器械身份、质量、安全、性能等的书面 / 电子 / 口头反馈 |核心原则
过程方法:将 QMS视为相互关联的过程集合,强调过程的顺序、交互及控制。
风险导向:风险仅涉及医疗器械安全性能及法规合规,需贯穿 QMS全流程。
法规合规:需识别并融入适用的国家 /地区法规要求(如注册、不良事件报告)。
全生命周期管控:覆盖从产品构思到报废的全阶段,上市后需通过监测持续改进。
3、质量管理体系(QMS)要求
通用要求
需建立文件化QMS,明确组织在供应链中的角色(如制造商、进口商)。采用风险基于控制的方法,确定QMS 过程的顺序、交互及控制准则。外程需纳入管控,签订质量协议,保留终责任,不得因外包转移合规义务。计算机软件(QMS用)需验证,变更后需再验证,验证深度与风险匹配。文档控制
必备文档:质量方针 / 目标、质量手册、QMS所需程序文件、医疗器械文件、记录。质量手册:需明确 QMS范围、排除条款及理由、过程交互描述。医疗器械文件:每个器械类型 /家族需建立专属文件,含产品描述、规格、生产 / 检验规程等。记录控制:需明确标识、存储、检索、保存期限(至少产品寿命期或放行后2 年)、处置要求;需保护机密健康信息。4、管理责任
高层承诺
高层需通过沟通法规重要性、建立质量方针 /目标、开展管理评审、保障资源等,证明对 QMS 的承诺。质量方针:需适应组织宗旨,包含合规承诺,为质量目标提供框架。质量目标:需可测量,与质量方针一致,覆盖相关职能和层级。组织与沟通
明确各岗位职责权限,确保质量相关工作的独立性和性。任命管理者代表:无论其他职责,需负责QMS 过程文件化、向高层报告 QMS 有效性、推广法规意识。内部沟通:建立机制,确保 QMS有效性相关信息的传递。管理评审
频次:按计划的间隔开展,需形成记录。输入:含反馈、投诉、法规变化、审核结果、纠正 /预防措施等 12 项内容。输出:含 QMS改进、产品改进、资源需求等决策。5、资源管理
人力资源
关键要求:从事影响产品质量工作的人员需具备教育、培训、技能、经验等胜任能力。培训管理:需制定培训计划,评估培训效果,保留教育、培训、技能记录。意识要求:确保员工知晓自身活动对质量目标的贡献、违规后果。基础设施
涵盖:厂房 /workspace、生产 /检验设备、运输 / 通信 / 信息系统。设备维护:需制定维护规程和间隔,保留维护记录(设备故障可能影响产品质量时)。工作环境
需明确环境要求(如温度、洁净度),若环境影响产品质量,需监测和控制。人员要求:若人员健康 / 清洁 /着装影响产品安全,需制定相关要求。污染控制:无菌器械需专项控制微生物 /颗粒物污染,维持装配 / 包装过程的洁净度。6、产品实现(核心模块)
策划与客户相关过程
产品实现策划:需确定质量目标、所需过程 / 文档 /资源、验证 / 确认活动、记录要求,建立风险管理制度。客户需求:确定客户明确要求、隐含要求、法规要求,签订合同前评审需求,确保组织有能力满足。沟通:建立与客户(产品信息、投诉)、监管机构(法规合规)的沟通机制。设计与开发(全流程控制)
| 阶段 |关键要求 || 输入 | 含功能 / 性能 /安全要求、法规标准、风险管理输出,需完整、无冲突、可验证 || 输出 | 满足输入要求,含采购 /生产信息、产品验收准则、安全使用特性 || 评审 |关键阶段开展系统评审,参与人员含相关职能代表,保留记录 || 验证 |确保输出满足输入,需制定验证计划(含抽样理由),接口类产品需验证互联兼容性 || 确认 |确保产品满足预期用途,需用代表性产品(初始生产单元 / 批次),无菌 /植入器械需临床评价 || 转移 |验证设计输出适合生产,确保生产能力满足产品要求 || 变更控制 | 评估变更对产品功能 / 安全 /法规的影响,需评审、验证 / 确认、批准,保留记录 || 文件 | 每个器械类型 /家族需建立设计开发文件,含变更记录 |
采购管理
供应商评价:基于供应商提供产品的质量影响、风险等级,制定评价 / 选择 /再评价准则。采购信息:明确产品规格、验收要求、供应商人员资质、QMS要求,需在传递前确认充分性。进货验证:基于供应商评价结果和风险,开展检验 /验证,可在供应商现场验证,保留记录。生产与服务提供
清洁度:对需清洁 /无菌的产品,制定清洁度要求。无菌器械:需保留每批灭菌过程参数记录,确保可追溯至生产批次。过程验证:对无法通过后续监测验证的过程(如灭菌),需验证(含人员 /设备资格),定期再验证。过程控制:需策划并控制生产过程,含工艺参数监测、标识追溯、包装标签、产品放行。特殊要求:标识与追溯:产品全生命周期需标识状态(待检 / 合格/ 不合格),植入式器械需追溯组件、材料、生产环境。产品防护:制定存储、搬运、分销过程的防护要求,避免污染/ 损坏。监测设备控制
校准 /验证:按规定间隔或使用前校准,标准需可追溯至国际 / 国家标准,无标准时需记录校准依据。状态标识:需标识校准状态(合格 / 不合格 /准用)。软件验证:用于监测测量的软件需验证,变更后再验证。7、测量、分析与改进
监测与测量
反馈:收集生产及上市后反馈,作为风险管理输入。投诉处理:制定程序,含接收、记录、调查、报告监管机构、纠正措施等要求,未调查需记录理由。内部审核:按计划开展,审核员不得审核自身工作,需向受审核部门提出纠正措施,验证效果。产品 / 过程监测:监测产品特性(各阶段)和 QMS过程,确保满足要求。不合格品控制
控制要求:标识、隔离、评审、处置,保留非符合性及处置记录。处置方式:返工(需验证)、让步接收(需批准并符合法规)、报废。上市后不合格:需采取与影响程度匹配的措施,必要时发布咨询通知。数据分析
分析内容:含反馈、产品合规性、过程 /产品趋势、供应商表现、审核结果等。方法:需确定统计技术等分析方法,分析结果作为改进输入。改进
纠正措施:针对非符合性(含投诉),分析原因,制定并验证措施,确保不产生负面影响。预防措施:识别潜在非符合性原因,制定并验证措施,与风险程度匹配。8、附录(资料性)
附录 A:对比 ISO 13485:2016 与2003 版的差异(如新增设计开发转移、投诉处理条款)。附录 B:列出 ISO 13485:2016 与ISO 9001:2015 的条款对应关系,明确本标准为独立标准,不包含 ISO 9001的部分非法规相关要求。ICP许可证,网文许可证,节目制作许可证,三类医疗器械许可证,建筑类许可证